His标签蛋白纯化磁珠 HisSep Ni-NTA MagBeads
产品说明书
FAQ
COA
已发表文献
His-tag蛋白纯化磁珠是一种高容量的新型磁性微球产品,用于快速、高效的纯化 His标签融合蛋白。磁珠在磁场作用下直接从生物样品中可一步纯化出高达95%纯度的目的蛋白,极大的简化了纯化工艺和提高纯化效率。将含有His标签蛋白的细胞裂解物添加到MagBeads 中,让蛋白质与其充分结合,然后可从磁珠中洗脱分离出目的蛋白。
与传统柱层析方法相比,使用磁珠纯化His标签蛋白无需控制上样流速和多次离心样品,也不需要昂贵的层析和离心设备。样品与磁珠的结合以及目的蛋白与磁珠的分离简单、快捷,而且更容易实现高通量、自动化的蛋白纯化方法。适合科研和工业客户高通量地进行组氨酸标签蛋白的纯化。
该磁珠以4%琼脂糖凝胶为基质通过化学方法偶联了四配位的氮川三乙酸(NTA),螯合镍离子(Ni2+)后,可以形成非常稳定的八面体结构,镍离子处于八面体的中心,这样的结构很有效的保护了镍离子免受小分子的进攻更加稳定。
His标签蛋白纯化磁珠广泛适用于细菌、酵母、昆虫和哺乳动物细胞等分泌或胞内表达的可溶性组氨酸标签蛋白,也可用于变性蛋白的纯化(包涵体需变性后再进行纯化)。
产品性质
|
基质 |
磁性琼脂糖微球 |
|
载量 |
> 40 mg 6×His-tagged protein/mL磁珠 |
|
粒径 |
30-100 μm |
|
磁珠浓度 |
磁珠悬浮于保护液中,含量为20%(V/V) |
|
储存缓冲液 |
含20%乙醇的1×PBS |
运输和保存方法
冰袋运输。4℃长期储存,有效期2年。
注意事项
1.磁珠保存过程中避免冷冻、干燥和高速离心等操作。
2.磁珠使用前,请充分震荡,使磁珠保持均匀的悬浮状态。
3.使用过的磁珠重复使用时,建议纯化同一种蛋白,纯化不同种蛋白时,建议使用新磁珠,以避免交叉污染。
4.为了您的安全和健康,请穿实验服并戴一次性手套操作。
5.本产品仅作科研用途!
使用方法
一、缓冲液配制
1.缓冲液使用基本原理:低咪唑上样,高咪唑洗脱,或者高pH上样,低pH洗脱。
2.Buffer在使用前最好用0.22 μm或者0.45 μm滤膜过滤除菌。
3.可溶性蛋白纯化所需缓冲液及配方详见附表1,包涵体蛋白纯化所需缓冲液及配方详见附表2和表3。
二、样本制备
2.1细菌或酵母表达的蛋白
1)将培养液转移到离心杯中,7,000 rpm (7,500 xg),离心15 min收集菌体,然后按照菌体:Lysis Buffer=1: 10 (W/V)加入Lysis Buffer,加入终浓度为1 mM的PMSF。同时可加入其他蛋白酶抑制剂,但不能影响目的蛋白与磁珠的结合。
2)加入溶菌酶,使其工作浓度为0.2-0.4 mg/mL。如果表达的宿主细胞内含pLysS或pLysE,可以不加溶菌酶。
3)将菌体沉淀悬浮起来,(如果菌液浓度高,也可考虑加入10 μg/mL RNase A和5 μg/mL DNase I),混匀,冰上超声破碎细胞,至菌液基本保持澄清。
4)将澄清的破碎液转移至离心管中,10,000 rpm (15,000 xg),4℃离心20-30 min。 取上清,置于冰上备用或-20℃保存。
2.2酵母、昆虫和哺乳细胞分泌表达可溶性蛋白
1)将细胞培养液转移至离心杯中,5,000 rpm (3,800 xg),离心10 min,收集菌体得上清,如上清中不含EDTA、组氨酸和还原剂等物质,即可直接使用;如含有EDTA、组氨酸和还原剂等物质,需用Lysis Buffer透析才能上样。
2)对于大量体积的上清,需加入硫酸铵沉淀浓缩后,然后用Lysis Buffer透析后才能上样。
2.3包涵体蛋白纯化(变性条件)
1)将培养液转移到离心杯中,7,000 rpm (7,500 xg),离心15 min收集菌体,去掉上清。
2)按照菌体:Lysis buffer(不含8M尿素)=1:10 (W/V)将菌体悬浮起来,混匀,冰浴超声破碎。
3)将破碎液转移至离心管中,10,000 rpm (15,000 xg),4℃离心20-30 min。去掉上清,步骤2和3可以重复一次。
4)按照菌体:Lysis buffer(含8M尿素)=1:10 (w/v)的比例将包涵体充分悬浮。
三、磁珠预处理
3.1 准备
将磁珠充分混匀,使用移液器取适量的磁珠悬浮液,置于离心管中,将离心管置于磁力架上,待溶液变澄清后,用移液器吸弃上清。
3.2平衡
将离心管从磁力架上取下来,加入与悬浮液等体积的Lysis Buffer,使用枪头反复吹打5-10次,将离心管置于磁分离器上,待溶液变澄清后,用移液器吸弃清液,重复洗涤2次。
四、磁珠与目的蛋白结合
4.1 结合
将含有目的蛋白的上清液加入到处理好的磁珠中,颠倒混匀。将离心管置于混合仪上,室温旋转孵育30 min (如果目标蛋白不稳定,建议2-8℃下孵育1 h)。
4.2 洗杂
将离心管置于磁分离器,待溶液变澄清后,用移液器移出上清液,保留上清液,以备取样检测。向离心管中加入2倍悬浮液体积的Wash Buffer,使用枪头反复吹打5-10次,将离心管置于磁分离器上,待溶液变澄清后,用移液器吸取上清液,保留,以备取样检测。重复上述步骤2次。
4.3 洗脱
建议将3-5倍磁珠体积的Elution Buffer加入到离心管中,使用移液器轻轻吹打3-5次,混匀,将离心管置于磁分离器上,待溶液变澄清后,用移液器吸取上清液,即为目的蛋白。如有需要,可以重复上述步骤1次,以提高目的蛋白的回收量。用户也可根据实验结果调整缓冲液中的咪唑浓度。
五、磁珠保存
1. 向装有磁珠的离心管中加入1 mL Elution Buffer,用移液器反复吹打3-5次,使磁珠充分悬浮,然后置于磁分离器,吸弃上清,重复该操作2次。
2. 向离心管中加入1 mL去离子水,用移液器反复吹打3-5次,使磁珠充分悬浮,然后置于磁分离器,吸弃上清,重复该操作2次。
3. 向离心管中加入含20%乙醇的1×PBS,使总体积为磁珠初始悬浮液体积,保存于2-8 ℃。
六、SDS-PAGE 检测
将纯化得到的样品(包括原始样品、流出组分、洗杂及洗脱组分)使用SDS-PAGE检测纯化效果。
表1. 可溶性His标签蛋白纯化所需缓冲液及配方
|
缓冲液名称 |
配方 |
配制1L溶液所需各种试剂量 |
|
Lysis Buffer |
50 mM NaH2PO4 300 mM NaCl 10 mM imidazole NaOH调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
NaH2PO4 ·2H2O 7.80 g NaCl 17.54 g Imidazole 0.68 g
|
|
Wash Buffer |
50 mM NaH2PO4 300 mM NaCl 20 mM imidazole NaOH调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
NaH2PO4 ·2H2O 7.80 g NaCl 17.54 g Imidazole 1.36 g
|
|
Elution Buffer |
50 mM NaH2PO4 300 mM NaCl 250 mM imidazole NaOH调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
NaH2PO4 ·2H2O 7.80 g NaCl 17.54 g Imidazole 17.0 g
|
以上缓冲液适用于多数His标签蛋白的纯化,客户也可根据实验结果调整缓冲液中的咪唑浓度。
表2. 包涵体His标签蛋白纯化所需缓冲液及配方,pH洗脱方式
|
缓冲液名称 |
配方 |
配制1L溶液所需各种试剂量 |
|
Lysis Buffer |
8 M Urea 100 mM NaH2PO4 100 mM Tris·HCl 盐酸溶液调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
Urea 480.50 g NaH2PO4 ·H2O 13.80 g Tris·Cl 12.10 g
|
|
Wash Buffer |
8 M Urea 100 mM NaH2PO4 100 mM Tris·HCl 盐酸溶液调pH至6.3,0.22 µm或0.45 µm过滤除菌 |
Urea 480.50 g NaH2PO4 ·H2O 13.80 g Tris·Cl 12.10 g |
|
Elution Buffer |
8 M Urea 100 mM NaH2PO4 100 mM Tris·HCl 盐酸溶液调pH至4.5,0.22 µm或0.45 µm过滤除菌 |
Urea 480.50 g NaH2PO4 ·H2O 13.80 g Tris·Cl 12.10 g |
表3. 包涵体His标签蛋白纯化所需缓冲液及配方,咪唑洗脱方式
|
缓冲液名称 |
配方 |
配制1L溶液所需各种试剂量 |
|
Lysis Buffer |
8 M Urea 50 mM NaH2PO4 300 mM NaCl 10 mM imidazole NaOH调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
Urea 480.50 g NaH2PO4 ·2H2O 7.80 g NaCl 17.54 g Imidazole 0.68 g |
|
Wash Buffer |
8 M Urea 50 mM NaH2PO4 300 mM NaCl 20 mM imidazole NaOH调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
Urea 480.50 g NaH2PO4 ·2H2O 7.80 g NaCl 17.54 g Imidazole 1.36 g |
|
Elution Buffer |
8 M Urea 50 mM NaH2PO4 300 mM NaCl 250 mM imidazole NaOH调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
Urea 480.50 g NaH2PO4 ·2H2O 7.80 g NaCl 17.54 g Imidazole 17.0 g |
表4. Ni NTA Magarose Beads试剂耐受情况
|
试剂种类 |
浓度 |
|
还原剂 |
5 mM DTE 1 mM DTT 20 mM β-mercaptoethanol 5 mM TCEP 10 mM reduced glutathione |
|
变性剂 |
8 M urea 6 M Gua-HCl |
|
去污剂 |
2% TritonTM X-100, nonionic 2% TweenTM20, nonionic 2% NP-40, nonionic 2% Cholate, anionic 1% CHAPS, zwitterionic |
|
其他类 |
500 mM imidazole 20% ethanol 50% glycerol 100 mM Na2SO4 1.5 M NaCl 1 mM EDTA 60 mM citrate |
HB220315
His-tag蛋白纯化磁珠是一种高容量的新型磁性微球产品,用于快速、高效的纯化 His标签融合蛋白。磁珠在磁场作用下直接从生物样品中可一步纯化出高达95%纯度的目的蛋白,极大的简化了纯化工艺和提高纯化效率。将含有His标签蛋白的细胞裂解物添加到MagBeads 中,让蛋白质与其充分结合,然后可从磁珠中洗脱分离出目的蛋白。
与传统柱层析方法相比,使用磁珠纯化His标签蛋白无需控制上样流速和多次离心样品,也不需要昂贵的层析和离心设备。样品与磁珠的结合以及目的蛋白与磁珠的分离简单、快捷,而且更容易实现高通量、自动化的蛋白纯化方法。适合科研和工业客户高通量地进行组氨酸标签蛋白的纯化。
该磁珠以4%琼脂糖凝胶为基质通过化学方法偶联了四配位的氮川三乙酸(NTA),螯合镍离子(Ni2+)后,可以形成非常稳定的八面体结构,镍离子处于八面体的中心,这样的结构很有效的保护了镍离子免受小分子的进攻更加稳定。
His标签蛋白纯化磁珠广泛适用于细菌、酵母、昆虫和哺乳动物细胞等分泌或胞内表达的可溶性组氨酸标签蛋白,也可用于变性蛋白的纯化(包涵体需变性后再进行纯化)。
产品性质
|
基质 |
磁性琼脂糖微球 |
|
载量 |
> 40 mg 6×His-tagged protein/mL磁珠 |
|
粒径 |
30-100 μm |
|
磁珠浓度 |
磁珠悬浮于保护液中,含量为20%(V/V) |
|
储存缓冲液 |
含20%乙醇的1×PBS |
运输和保存方法
冰袋运输。4℃长期储存,有效期2年。
注意事项
1.磁珠保存过程中避免冷冻、干燥和高速离心等操作。
2.磁珠使用前,请充分震荡,使磁珠保持均匀的悬浮状态。
3.使用过的磁珠重复使用时,建议纯化同一种蛋白,纯化不同种蛋白时,建议使用新磁珠,以避免交叉污染。
4.为了您的安全和健康,请穿实验服并戴一次性手套操作。
5.本产品仅作科研用途!
使用方法
一、缓冲液配制
1.缓冲液使用基本原理:低咪唑上样,高咪唑洗脱,或者高pH上样,低pH洗脱。
2.Buffer在使用前最好用0.22 μm或者0.45 μm滤膜过滤除菌。
3.可溶性蛋白纯化所需缓冲液及配方详见附表1,包涵体蛋白纯化所需缓冲液及配方详见附表2和表3。
二、样本制备
2.1细菌或酵母表达的蛋白
1)将培养液转移到离心杯中,7,000 rpm (7,500 xg),离心15 min收集菌体,然后按照菌体:Lysis Buffer=1: 10 (W/V)加入Lysis Buffer,加入终浓度为1 mM的PMSF。同时可加入其他蛋白酶抑制剂,但不能影响目的蛋白与磁珠的结合。
2)加入溶菌酶,使其工作浓度为0.2-0.4 mg/mL。如果表达的宿主细胞内含pLysS或pLysE,可以不加溶菌酶。
3)将菌体沉淀悬浮起来,(如果菌液浓度高,也可考虑加入10 μg/mL RNase A和5 μg/mL DNase I),混匀,冰上超声破碎细胞,至菌液基本保持澄清。
4)将澄清的破碎液转移至离心管中,10,000 rpm (15,000 xg),4℃离心20-30 min。 取上清,置于冰上备用或-20℃保存。
2.2酵母、昆虫和哺乳细胞分泌表达可溶性蛋白
1)将细胞培养液转移至离心杯中,5,000 rpm (3,800 xg),离心10 min,收集菌体得上清,如上清中不含EDTA、组氨酸和还原剂等物质,即可直接使用;如含有EDTA、组氨酸和还原剂等物质,需用Lysis Buffer透析才能上样。
2)对于大量体积的上清,需加入硫酸铵沉淀浓缩后,然后用Lysis Buffer透析后才能上样。
2.3包涵体蛋白纯化(变性条件)
1)将培养液转移到离心杯中,7,000 rpm (7,500 xg),离心15 min收集菌体,去掉上清。
2)按照菌体:Lysis buffer(不含8M尿素)=1:10 (W/V)将菌体悬浮起来,混匀,冰浴超声破碎。
3)将破碎液转移至离心管中,10,000 rpm (15,000 xg),4℃离心20-30 min。去掉上清,步骤2和3可以重复一次。
4)按照菌体:Lysis buffer(含8M尿素)=1:10 (w/v)的比例将包涵体充分悬浮。
三、磁珠预处理
3.1 准备
将磁珠充分混匀,使用移液器取适量的磁珠悬浮液,置于离心管中,将离心管置于磁力架上,待溶液变澄清后,用移液器吸弃上清。
3.2平衡
将离心管从磁力架上取下来,加入与悬浮液等体积的Lysis Buffer,使用枪头反复吹打5-10次,将离心管置于磁分离器上,待溶液变澄清后,用移液器吸弃清液,重复洗涤2次。
四、磁珠与目的蛋白结合
4.1 结合
将含有目的蛋白的上清液加入到处理好的磁珠中,颠倒混匀。将离心管置于混合仪上,室温旋转孵育30 min (如果目标蛋白不稳定,建议2-8℃下孵育1 h)。
4.2 洗杂
将离心管置于磁分离器,待溶液变澄清后,用移液器移出上清液,保留上清液,以备取样检测。向离心管中加入2倍悬浮液体积的Wash Buffer,使用枪头反复吹打5-10次,将离心管置于磁分离器上,待溶液变澄清后,用移液器吸取上清液,保留,以备取样检测。重复上述步骤2次。
4.3 洗脱
建议将3-5倍磁珠体积的Elution Buffer加入到离心管中,使用移液器轻轻吹打3-5次,混匀,将离心管置于磁分离器上,待溶液变澄清后,用移液器吸取上清液,即为目的蛋白。如有需要,可以重复上述步骤1次,以提高目的蛋白的回收量。用户也可根据实验结果调整缓冲液中的咪唑浓度。
五、磁珠保存
1. 向装有磁珠的离心管中加入1 mL Elution Buffer,用移液器反复吹打3-5次,使磁珠充分悬浮,然后置于磁分离器,吸弃上清,重复该操作2次。
2. 向离心管中加入1 mL去离子水,用移液器反复吹打3-5次,使磁珠充分悬浮,然后置于磁分离器,吸弃上清,重复该操作2次。
3. 向离心管中加入含20%乙醇的1×PBS,使总体积为磁珠初始悬浮液体积,保存于2-8 ℃。
六、SDS-PAGE 检测
将纯化得到的样品(包括原始样品、流出组分、洗杂及洗脱组分)使用SDS-PAGE检测纯化效果。
表1. 可溶性His标签蛋白纯化所需缓冲液及配方
|
缓冲液名称 |
配方 |
配制1L溶液所需各种试剂量 |
|
Lysis Buffer |
50 mM NaH2PO4 300 mM NaCl 10 mM imidazole NaOH调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
NaH2PO4 ·2H2O 7.80 g NaCl 17.54 g Imidazole 0.68 g
|
|
Wash Buffer |
50 mM NaH2PO4 300 mM NaCl 20 mM imidazole NaOH调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
NaH2PO4 ·2H2O 7.80 g NaCl 17.54 g Imidazole 1.36 g
|
|
Elution Buffer |
50 mM NaH2PO4 300 mM NaCl 250 mM imidazole NaOH调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
NaH2PO4 ·2H2O 7.80 g NaCl 17.54 g Imidazole 17.0 g
|
以上缓冲液适用于多数His标签蛋白的纯化,客户也可根据实验结果调整缓冲液中的咪唑浓度。
表2. 包涵体His标签蛋白纯化所需缓冲液及配方,pH洗脱方式
|
缓冲液名称 |
配方 |
配制1L溶液所需各种试剂量 |
|
Lysis Buffer |
8 M Urea 100 mM NaH2PO4 100 mM Tris·HCl 盐酸溶液调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
Urea 480.50 g NaH2PO4 ·H2O 13.80 g Tris·Cl 12.10 g
|
|
Wash Buffer |
8 M Urea 100 mM NaH2PO4 100 mM Tris·HCl 盐酸溶液调pH至6.3,0.22 µm或0.45 µm过滤除菌 |
Urea 480.50 g NaH2PO4 ·H2O 13.80 g Tris·Cl 12.10 g |
|
Elution Buffer |
8 M Urea 100 mM NaH2PO4 100 mM Tris·HCl 盐酸溶液调pH至4.5,0.22 µm或0.45 µm过滤除菌 |
Urea 480.50 g NaH2PO4 ·H2O 13.80 g Tris·Cl 12.10 g |
表3. 包涵体His标签蛋白纯化所需缓冲液及配方,咪唑洗脱方式
|
缓冲液名称 |
配方 |
配制1L溶液所需各种试剂量 |
|
Lysis Buffer |
8 M Urea 50 mM NaH2PO4 300 mM NaCl 10 mM imidazole NaOH调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
Urea 480.50 g NaH2PO4 ·2H2O 7.80 g NaCl 17.54 g Imidazole 0.68 g |
|
Wash Buffer |
8 M Urea 50 mM NaH2PO4 300 mM NaCl 20 mM imidazole NaOH调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
Urea 480.50 g NaH2PO4 ·2H2O 7.80 g NaCl 17.54 g Imidazole 1.36 g |
|
Elution Buffer |
8 M Urea 50 mM NaH2PO4 300 mM NaCl 250 mM imidazole NaOH调pH至8.0,0.22 µm或0.45 µm过滤除菌 |
Urea 480.50 g NaH2PO4 ·2H2O 7.80 g NaCl 17.54 g Imidazole 17.0 g |
表4. Ni NTA Magarose Beads试剂耐受情况
|
试剂种类 |
浓度 |
|
还原剂 |
5 mM DTE 1 mM DTT 20 mM β-mercaptoethanol 5 mM TCEP 10 mM reduced glutathione |
|
变性剂 |
8 M urea 6 M Gua-HCl |
|
去污剂 |
2% TritonTM X-100, nonionic 2% TweenTM20, nonionic 2% NP-40, nonionic 2% Cholate, anionic 1% CHAPS, zwitterionic |
|
其他类 |
500 mM imidazole 20% ethanol 50% glycerol 100 mM Na2SO4 1.5 M NaCl 1 mM EDTA 60 mM citrate |
HB220315
Q:目标蛋白回收率低怎么办?
A:1)延长粗蛋白与磁珠的孵育时间;
2)适当降低样品溶液和Binding/Wash Buffer中的Imidazole浓度;
3)添加合适的蛋白酶抑制剂,防止目标蛋白降解;
4)增加磁珠用量;
5)延长洗脱目标蛋白的时间或增加洗脱次数;
6)在样品溶液和其它缓冲液中添加表面活性剂等物质。
Q:如何提高目标蛋白纯度?
A:1)适当提高样品溶液和Binding/Wash Buffer中的Imidazole和NaCl浓度;
2)在纯化过程中添加合适的蛋白酶抑制剂,防止目标蛋白降解;
3)在样品溶液和缓冲液中加入表面活性剂等物质;
4)延长清洗的时间,增加清洗次数;
5)采用梯度Imidazole浓度洗脱目标蛋白。
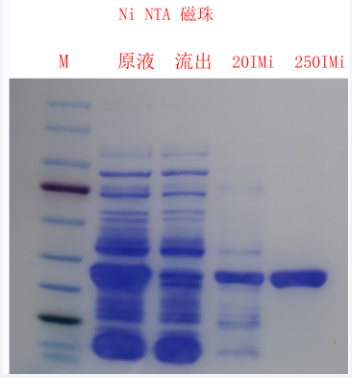
Q:是否有测试结果?
A:有,见下图
[1] Xu G, Han S, Huo C, et al. Signaling specificity in the c-di-GMP-dependent network regulating antibiotic synthesis in Lysobacter. Nucleic Acids Res. 2018;46(18):9276-9288. doi:10.1093/nar/gky803(IF:11.561)